細胞分子生物学講座について
講座概要
細胞分子生物学講座は分子機能制御学分野と細胞生理学分野からなり、口腔医学の理解に欠かせない細胞の仕組みと生体の機能、さらに薬物と生体との相互作用などの授業を受け持っています。教員は9名(2021年4月時点)で学生への教育を行うとともに生命現象の解明を目指した研究を進めています。
主任教授挨拶
細胞分子生物学講座 分子機能制御学分野 教授 八田光世
細胞分子生物学講座は「分子機能制御学分野」と「細胞生理学分野」の2分野で構成されています。分子機能制御学分野は生物系の基礎科目(細胞生物学)と薬物療法の基盤となる専門基礎科目(薬理学)、細胞生理学分野は生体機能の維持・調節に関する専門基礎科目(生理学)を担当しています。研究面では生命現象の分子メカニズム解明を目指し、「アポトーシス」、「遺伝子発現と細胞フェノタイプ」、「骨代謝調節機構」に着目した研究テーマを展開しています。口腔医学研究センターを活用し、大学院生や共同研究者とともに活発な研究活動を行なっています。
それぞれの名称をクリックすると、詳細情報に移動します。
細胞生理学分野
私たちは・・・
骨や歯を構成・調節する細胞を用いて細胞、分子レベルでの骨代謝制御機構についてイオン輸送体を中心に研究を行っています。また、学部生、大学院生に対して、分子、細胞、生体レベルにおける生命の維持と調節機構に関して教育しています。
骨は・・・
骨を作る細胞や吸収する細胞など、多くの細胞によってその大きさや強さが維持されています。このうち骨を吸収する細胞を破骨細胞と呼びます。破骨細胞は骨表面にぴったり貼り付いて塩酸を出し、骨を溶かしていきます。溶かし終えると足を出して、新しい場所へ移動していきます。
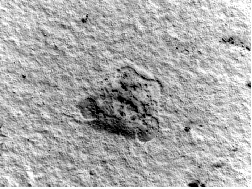
只今作業中・・・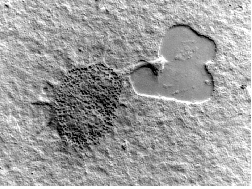
只今移動中・・・
研究テーマ
骨硬組織の細胞を用いた骨代謝調節機構の研究
(1)破骨細胞の骨吸収調節機構の研究
破骨細胞の受容体・膜イオン輸送・細胞内情報伝達・H+放出・骨吸収などの関係を、電気生理学的手法や細胞内Ca2+濃度および細胞内pH測定法、免疫組織学的手法および分子生物学的手法を用いて検討しています。こうした研究によって破骨細胞の分化増殖機構や骨吸収調節機構を明らかにし、骨粗鬆症や歯周病による病的骨吸収の治療に応用したいと考えています。
破骨細胞は吸盤のように骨の表面にぴったりくっつき、酸を分泌して骨を溶かします。この仕組みは非常に複雑で無数の細胞内分子が協力して働いています。私たちはその中でも、イオンチャネルと酸分泌機構に的を絞って研究しています。
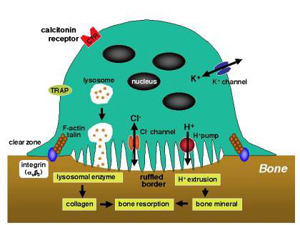
破骨細胞による骨の吸収
(2)骨細胞による骨メカニカルストレス受容機構の研究
骨への機械的刺激の受容機構を解明するため、骨組織の90%以上を占める骨細胞を用い、それに機械的刺激を与えた時に起こる変化を、イオンチャネルの活性化や細胞内Ca2+濃度の変化、および、分子生物学的な手法を用いて検討しています。骨細胞は骨の中に埋まっており、移動することができません。また、取り出すことが難しく、研究しにくいため、性質もよくわかっていません。私たちは骨の中から上手に骨細胞を取りだし、その性質を調べています。今までに骨細胞は浸透圧や外力に反応してイオン電流が変化することを見つけました。
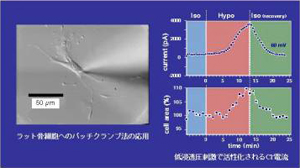
骨細胞とイオン電流
(3)ヒト破歯細胞を用いたヒト歯牙交換の調節機構の研究
破歯細胞の機能的な性質やヒト乳歯の生理的歯根吸収の調節機構はよくわかっていません。ヒト乳歯の交換期に出現する破歯細胞を抜去乳歯より単離し、その機能的性質や分化増殖機構を検討することにより、歯牙交換の調節機序を解明したいと考えています。抜け落ちた乳歯を酒石酸抵抗性酸性フォスファターゼ(TRAP)という酵素で染めると歯根だけが紫色に染まります。さらに顕微鏡で詳しく調べると破歯細胞と呼ばれる細胞だけが紫色に染まっているのが観察できます。この細胞は歯根の表面に接着し、歯根を溶かして乳歯の吸収が起こります。歯根が吸収されて初めて正常に永久歯が生えることができるようになります。
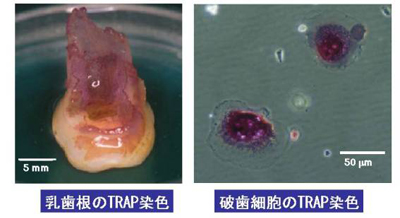
乳歯の歯根吸収と破歯細胞の存在
細胞生理学分野 所属教員
| 教授 | 藤田 亜美 |
|---|---|
| 准教授 | 鍛治屋 浩 |
| 講師 | 進 正史 |
分子機能制御学分野
私たちは・・・
分子機能制御学分野は生体の機能に関する授業のうち、薬理学や生物学に関連した授業を受け持っています。私たちの体には病気から回復させる復元力が元々備わっています。遺伝子に傷が付いても大事にならないうちにその傷を治す仕組みが細胞の中に備わっています。また、物質の中には元々備わっている復元力を強めたり、弱めたりする作用を持ったものがあり、それを薬として利用して病気を治しています。私たちはこうした生体の働きを研究しています。
分子機能制御学とは・・・
平成13年4月から始まった組織改革に伴って、旧生物学講座と旧歯科薬理学講座の両方の教育・研究を表している名称として名付けられました。
教育面では、1年生の「基礎理科」、「細胞生物学」、2年生の「分子生物学」、「薬理学」、「細胞分子生物学実習Ⅰ」、3年生の「口腔薬理学」、「臨床薬理学」、「細胞分子生物学実習Ⅱ」、「基礎研究演習」などの講義・演習・実習を担当しています。また、入学直前、臨床実習前ならびに最終学年の教育にも携わっています。
研究面では、生体の最小機能単位であるタンパク分子やその合成にかかわる遺伝子の機能を研究し、分子機能を制御することで疾患治療にアプローチしたいと考えています。研究室のドアはいつも開かれており、用がなくても気軽に入れるようにしていますので、是非遊びに来て下さい。
研究テーマ
日高グループ
1.遺伝子を護るアポトーシスの分子機構
私たちのからだを構成する細胞はゲノム上に2万個以上の遺伝子を持っています。遺伝子に変異が生じ、それがうまく働かなくなるとがんや遺伝病などの病気を発症することがあります。生体はそれを抑えるために種々の防御機能をもっています。その中の一つアポトーシス(細胞死)は、DNA上に変異を引き起こすような傷が生じた細胞を積極的に細胞死に導くことで、遺伝子を突然変異から護っています。私たちは、人為的にDNAの修復遺伝子を欠損させ遺伝子に傷が起こりやすくなった細胞を用いて、アポトーシス誘導の分子機構を研究しています。
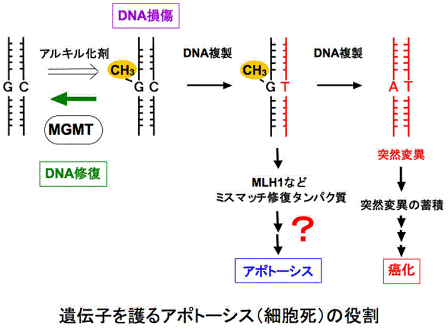
2.発がん抑制におけるアポトーシスの役割
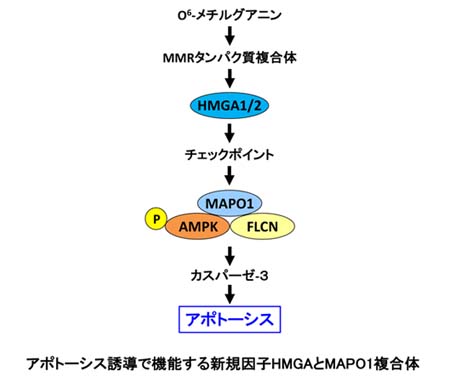
私たちは遺伝子トラップ法を用いてアポトーシスに関わる遺伝子を探索し、新規にMapo1 (O6-methylguanine-induced apoptosis 1)/FNIP2を同定しました。MAPO1は細胞内で発がん抑制タンパク質であるFLCN、そして、エネルギーセンサーであるAMPKの両者と複合体を形成して機能しています。アポトーシスの誘導過程において、MAPO1はユビキチン・プロテアソームによる分解から逃れて自らを安定化すると同時に、AMPKの活性化を制御し、アポトーシスの実行因子であるカスパーゼ3の活性化を引き起こします。また、非ヒストンのクロマチン結合タンパク質であるHMGAファミリータンパク質が新規のアポトーシス誘導因子として機能していることも見出しました。そこで、クロマチン動態によるアポトーシス誘導の制御機構にも注目して研究を進めています。がん細胞は正常細胞に比べてよく増殖するので、増殖の盛んな細胞を選択的にアポトーシスによって死滅させることが出来れば制がんの目的にも応用できるのではと期待しています。
八田グループ
私たちは、生命活動の基盤である遺伝子発現制御メカニズムの解明を主軸とし、特異的なDNA塩基配列に結合して転写調節に働く転写因子、さらにDNAメチル化やヒストン修飾などエピジェネティック制御に着目した研究活動をおこなっています。今後さらに、遺伝子発現制御を介した細胞フェノタイプ決定メカニズムの解明つまり細胞制御へと研究を発展させる計画です。これらの研究は発生・恒常性の維持および疾患の病態メカニズムの理解さらに疾患治療・細胞医療に繋がる基礎研究であり、医学の発展に寄与するものと考えています。
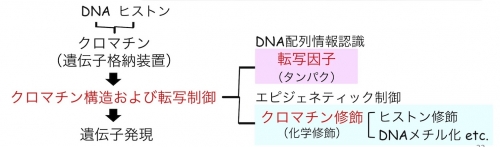
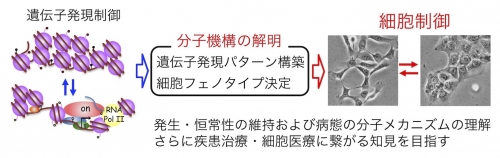
1.真核細胞における転写制御メカニズムの解明
2.ヒストン/DNAの化学修飾とクロマチン構造制御に関する研究
3.上皮細胞のフェノタイプ転換を制御する分子機構に関する研究
分子機能制御学分野 所属教員
| 教授 | 日髙 真純 |
|---|---|
| 教授 | 八田 光世 |
| 講師 | 藤兼 亮輔 |
| 講師 | 長岡 良礼 |
| 助教 | 武石 幸容 |



